
वर्ष 2022 के चिकित्सा नोबेल पुरस्कारों का ऐलान सोमवार 2 अक्टूबर 2023 को किया गया है। इस बार यह पुरस्कार कैटालिन कारिको (Katalin Karikó ) और ड्रू वीसमैन (Drew Weissman) को मिला है
कैरोलिंस्का इंस्टीट्यूट में नोबेल असेंबली ने फिजियोलॉजी या मेडिसिन में 2023 का नोबेल पुरस्कार संयुक्त रूप से कैटालिन कारिको और ड्रू वीसमैन को
“न्यूक्लियोसाइड बेस संशोधनों से संबंधित उनकी खोजों के लिए देने का फैसला किया है, जिसने सीओवीआईडी -19 के खिलाफ प्रभावी एमआरएनए टीकों के विकास को सक्षम किया है।”
दो नोबेल पुरस्कार विजेताओं की खोजें 2020 की शुरुआत में शुरू हुई महामारी के दौरान सीओवीआईडी -19 के खिलाफ प्रभावी एमआरएनए टीके विकसित करने के लिए महत्वपूर्ण थीं।
उन्होंने अपने अभूतपूर्व निष्कर्षों के माध्यम से, जिसने मूल रूप से हमारी समझ को बदल दिया है कि एमआरएनए हमारी प्रतिरक्षा प्रणाली के साथ कैसे संपर्क करता है। दोनों नोबेल पुरस्कार विजेताओं ने आधुनिक समय में मानव स्वास्थ्य के लिए सबसे बड़े खतरों में से एक के दौरान अभूतपूर्व दर से टीका विकास के लिए योगदान दिया ।
कोविड 19 से पहले वैक्सीन का निर्माण
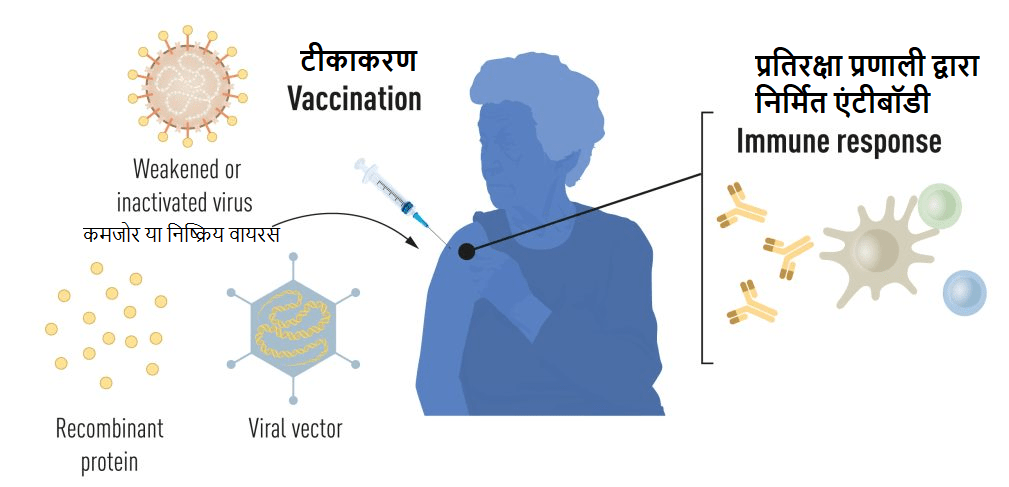
वैक्सीन या टीका एक विशेष वायरस के प्रति शरीर की प्रतिरक्षा प्रणाली को उत्तेजित करता जिससे उस वायरस से लड़ने के लिए एंटीबॉडी बनाते है। इससे शरीर को बाद में उस वायरस रोग के संपर्क में आने की स्थिति में बीमारी से लड़ने में मदद मिलती है। मारे गए या कमजोर वायरस पर आधारित टीके लंबे समय से उपलब्ध हैं, जिसका उदाहरण पोलियो, खसरा और पीले बुखार के खिलाफ टीके हैं। 1951 में, मैक्स थीलर को पीले बुखार का टीका विकसित करने के लिए फिजियोलॉजी या मेडिसिन में नोबेल पुरस्कार से सम्मानित किया गया था।
हाल के दशकों में आणविक जीव विज्ञान में प्रगति के लिए संपूर्ण वायरस के बजाय छोटे वायरल घटकों पर आधारित टीके विकसित किए गए हैं। इनमे पुरे वायरस की बजाये उसके घटको का प्रयोग होता है। इस प्रणाली में वायरल आनुवंशिक कोड के हिस्से, आमतौर पर वायरस की सतह पर पाए जाने वाले प्रोटीन का उपयोग टिका बनाने के लिए किया जाता है जो वायरस से लड़ने के लिए एंटीबॉडी के गठन को प्रेरित करता है। इसका उदाहरण हेपेटाइटिस बी वायरस और मानव पेपिलोमावायरस के खिलाफ टीके हैं। वैकल्पिक रूप से, वायरल आनुवंशिक कोड के कुछ हिस्सों को एक हानिरहित वाहक वायरस अर्थात , एक “वेक्टर” में ले जाया जा सकता है। इस पद्धति का उपयोग इबोला वायरस के खिलाफ टीकों में किया जाता है। जब वेक्टर टीके इंजेक्ट किए जाते हैं, तो हमारी कोशिकाओं में चयनित वायरल प्रोटीन उत्पन्न होता है, जो लक्षित वायरस के खिलाफ प्रतिरक्षा प्रतिक्रिया को उत्तेजित करता है।
संपूर्ण वायरस-, प्रोटीन- और वेक्टर-आधारित टीकों के उत्पादन के लिए बड़े पैमाने पर सेल कल्चर की आवश्यकता होती है। यह अधिक संसाधन वाली प्रक्रिया प्रकोप और महामारी के जवाब में तेजी से वैक्सीन उत्पादन की संभावनाओं को सीमित करती है। इसलिए, शोधकर्ताओं ने लंबे समय से सेल कल्चर से स्वतंत्र वैक्सीन प्रौद्योगिकियों को विकसित करने का प्रयास किया है। लेकिन यह चुनौतीपूर्ण साबित हुआ है ।
mRNA(एमआरएनए) टीके: एक नई आशा
हमारी कोशिकाओं में, डीएनए में एन्कोड की गई आनुवंशिक जानकारी मैसेंजर आरएनए (एमआरएनए) में स्थानांतरित हो जाती है, जिसका उपयोग प्रोटीन उत्पादन के लिए एक टेम्पलेट के रूप में किया जाता है। 1980 के दशक के दौरान, सेल कल्चर के बिना एमआरएनए के उत्पादन के लिए कुशल तरीके खोज लिए गए, जिन्हें इन विट्रो ट्रांसक्रिप्शन कहा जाता है। इस निर्णायक चरण ने कई क्षेत्रों में आणविक जीव विज्ञान अनुप्रयोगों के विकास को गति दी। वैक्सीन और चिकित्सीय उद्देश्यों के लिए एमआरएनए प्रौद्योगिकियों का उपयोग करने के विचार भी सामने आए, लेकिन कुछ बाधाएं बनी रहीं। इन विट्रो ट्रांसक्राइब्ड एमआरएनए को अस्थिर और वितरित करने के लिए चुनौतीपूर्ण माना जाता था, जिसके लिए एमआरएनए को को शरीर में वाहन करने के लिए परिष्कृत वाहक लिपिड (carrier lipid systems)सिस्टम के विकास की आवश्यकता होती थी। इसके अलावा, इन विट्रो-निर्मित एमआरएनए ने सूजन संबंधी प्रतिक्रियाओं को जन्म दिया। इसलिए, चिकित्सा उद्देश्यों के लिए एमआरएनए तकनीक विकसित करने का उत्साह शुरू में सीमित था।
इन सब बाधाओं ने हंगेरियन बायोकेमिस्ट कैटलिन कारिको को हतोत्साहित नहीं किया, जो चिकित्सा के लिए एमआरएनए का उपयोग करने के तरीकों को विकसित करने के लिए समर्पित थी। 1990 के दशक की शुरुआत में, जब वह पेंसिल्वेनिया विश्वविद्यालय में सहायक प्रोफेसर थीं, तो अपने प्रोजेक्ट के महत्व के बारे में अनुसंधान फंडर्स को समझाने में कठिनाइयों का सामना कर रही थी। इसके बावजूद वह एमआरएनए को चिकित्सीय के रूप में साकार करने के अपने दृष्टिकोण पर कायम रहीं। कारिको के विश्वविद्यालय में उनके नए सहयोगी इम्यूनोलॉजिस्ट ड्रू वीसमैन थे। उनकी रुचि डेंड्राइटिक कोशिकाओं में थी, जो प्रतिरक्षा निगरानी और वैक्सीन-प्रेरित प्रतिरक्षा प्रतिक्रियाओं को सक्रिय करने में महत्वपूर्ण कार्य करती हैं। नए विचारों से प्रेरित होकर, जल्द ही दोनों के बीच एक महत्वपूर्ण सहयोग शुरू हुआ, जिसमें इस बात पर ध्यान केंद्रित किया गया कि विभिन्न आरएनए प्रकार प्रतिरक्षा प्रणाली के साथ कैसे बातचीत करते हैं।
महत्वपूर्ण खोज
कारिको और वीसमैन ने देखा कि डेंड्राइटिक कोशिकाएं इन विट्रो ट्रांसक्राइब्ड एमआरएनए को एक परजीवी पदार्थ के रूप में पहचानती हैं, जिससे उनकी सक्रियता होती है और शरीर में सूजन उत्पन्न करने वाले संकेत अणु बनते है। उन्हें आश्चर्य हुआ कि इन विट्रो ट्रांसक्राइब्ड एमआरएनए को विदेशी के रूप में क्यों पहचाना गया जबकि स्तनधारी कोशिकाओं से एमआरएनए ने समान प्रतिक्रिया को जन्म नहीं दिया। कारिको और वीसमैन ने महसूस किया कि कुछ महत्वपूर्ण गुणों से विभिन्न प्रकार के एमआरएनए में अंतर करना चाहिए।
आरएनए में चार आधार होते हैं, जिन्हे संक्षिप्त रूप में ए, यू, जी और सी कहते है, ये आनुवंशिक कोड के अक्षर हैं और डीएनए में ए, टी, जी और सी के अनुरूप होते हैं। कारिको और वीसमैन जानते थे कि स्तनधारी कोशिकाओं से आरएनए में आधार अक्सर रासायनिक रूप से संशोधित(परिवर्तित) होते हैं, जबकि इन विट्रो ट्रांसक्राइब्ड एमआरएनए में ऐसा नहीं होता है। उन्हें आश्चर्य हुआ कि क्या इन विट्रो ट्रांसक्राइब्ड आरएनए में परिवर्तित आधारों की अनुपस्थिति अवांछित सूजन प्रतिक्रिया की व्याख्या कर सकती है? इसकी जांच करने के लिए, उन्होंने एमआरएनए के विभिन्न प्रकार तैयार किए, जिनमें से प्रत्येक के आधार में अद्वितीय रासायनिक परिवर्तन थे, जिन्हें उन्होंने डेंड्राइटिक कोशिकाओं तक पहुंचाया। परिणाम आश्चर्यजनक थे: जब आधार संशोधनों (परिवर्तनों) को एमआरएनए में शामिल किया गया तो सूजन संबंधी प्रतिक्रिया लगभग समाप्त हो गई थी। यह हमारी समझ में एक आदर्श स्तिथि कि हम जान गए थे कि कोशिकाएं एमआरएनए के विभिन्न रूपों को कैसे पहचानती हैं और किस तरह उन पर प्रतिक्रिया करती हैं। कारिको और वीसमैन को तुरंत समझ में आ गया कि एमआरएनए को चिकित्सा के रूप में उपयोग करने के लिए उनकी खोज का गहरा महत्व है। ये मौलिक परिणाम 2005 में, COVID-19 महामारी से पंद्रह साल पहले प्रकाशित हुए थे।
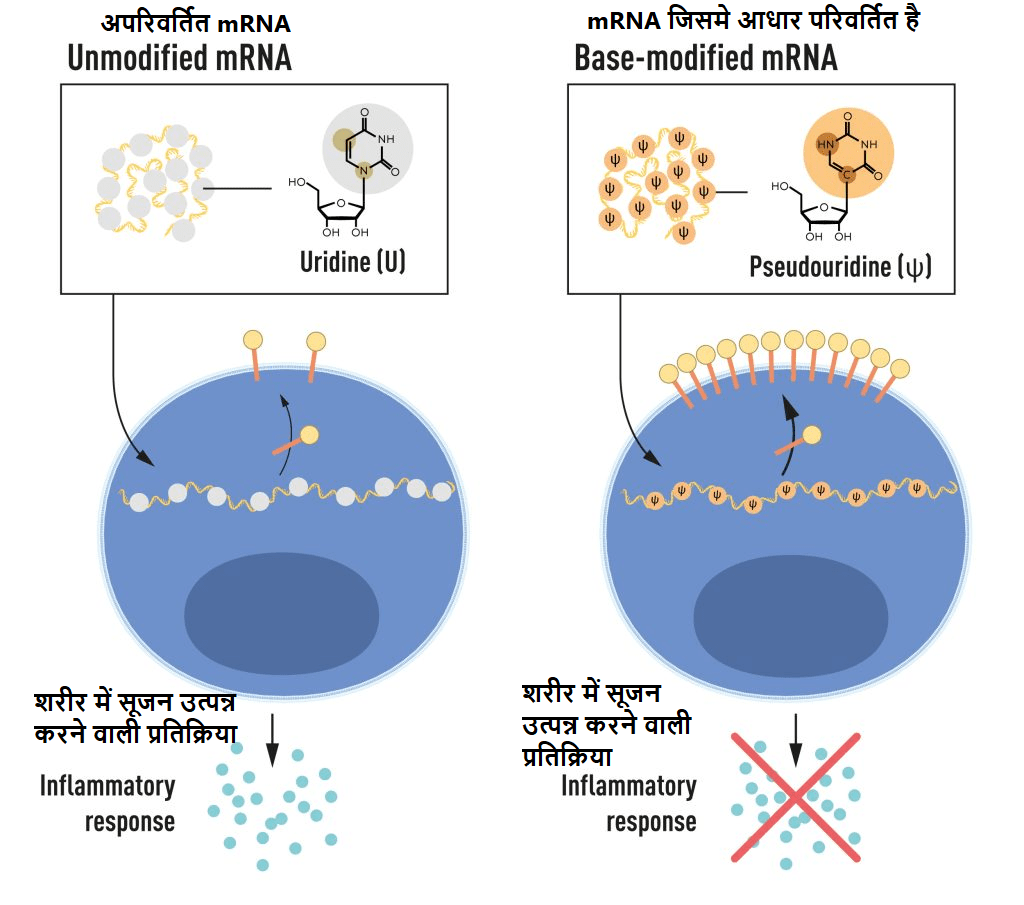
2008 और 2010 में प्रकाशित आगे के अध्ययनों में, कारिको और वीसमैन ने दिखाया कि आधार संशोधनों के साथ उत्पन्न एमआरएनए की डिलीवरी ने असंशोधित एमआरएनए की तुलना में प्रोटीन उत्पादन में उल्लेखनीय वृद्धि की है। यह प्रभाव प्रोटीन उत्पादन को नियंत्रित करने वाले एंजाइम की सक्रियता कम होने के कारण हुआ। अपनी खोजों के माध्यम से कि आधार संशोधनों ने सूजन संबंधी प्रतिक्रियाओं को कम किया और प्रोटीन उत्पादन में वृद्धि की, कारिको और वीसमैन ने एमआरएनए के चिकित्सीय अनुप्रयोगों के रास्ते में महत्वपूर्ण बाधाओं को समाप्त कर दिया था।
अंतत: एमआरएनए टीकों की क्षमता का एहसास हुआ
एमआरएनए प्रौद्योगिकी में रुचि बढ़ने लगी और 2010 में, कई कंपनियां इस पद्धति को विकसित करने पर काम कर रही थीं। जीका वायरस और एमईआरएस-सीओवी के खिलाफ टीके लगाए गए; इसका उत्तरार्द्ध SARS-CoV-2 से निकटता से संबंधित है। COVID-19 महामारी के फैलने के बाद, SARS-CoV-2 सतह प्रोटीन को एन्कोड करने वाले दो बेस-संशोधित mRNA टीके रिकॉर्ड गति से विकसित किए गए थे। इस प्रणाली लगभग 95% सुरक्षात्मक वाले टीके बनाये गए, और दोनों टीकों को दिसंबर 2020 की शुरुआत में अनुमोदित किया गया था।
जिस प्रभावशाली लचीलेपन और गति से एमआरएनए टीके विकसित किए जा सकते हैं, वह अन्य संक्रामक रोगों के खिलाफ टीकों के लिए भी नए प्लेटफॉर्म का उपयोग करने का मार्ग प्रशस्त करता है। भविष्य में, इस तकनीक का उपयोग चिकित्सीय प्रोटीन प्रदान करने और कुछ प्रकार के कैंसर के इलाज के लिए भी किया जा सकता है।
विभिन्न पद्धतियों के आधार पर SARS-CoV-2 के खिलाफ कई अन्य टीके भी तेजी से पेश किए गए, और साथ में, विश्व स्तर पर 13 बिलियन से अधिक COVID-19 वैक्सीन खुराक दी गई हैं। टीकों ने लाखों लोगों की जान बचाई है और कई लोगों में गंभीर बीमारी को रोका है, जिससे समाज खुलने और सामान्य स्थिति में लौटने में सक्षम हुए हैं। एमआरएनए में आधार संशोधनों के महत्व की अपनी मौलिक खोजों के माध्यम से, इस वर्ष के नोबेल पुरस्कार विजेताओं ने हमारे समय के सबसे बड़े स्वास्थ्य संकटों में से एक के दौरान इस परिवर्तनकारी विकास में महत्वपूर्ण योगदान दिया।
कातालिन कारिको (Katalin Karikó)

कातालिन कारिको का जन्म 1955 में हंगरी के स्ज़ोलनोक में हुआ था। उन्होंने 1982 में सेज्ड विश्वविद्यालय से पीएचडी प्राप्त की और 1985 तक सेज्ड में हंगेरियन एकेडमी ऑफ साइंसेज में पोस्टडॉक्टरल शोध किया। इसके बाद उन्होंने टेंपल यूनिवर्सिटी, फिलाडेल्फिया और यूनिवर्सिटी ऑफ हेल्थ साइंस, बेथेस्डा में पोस्टडॉक्टरल शोध किया। 1989 में, उन्हें पेंसिल्वेनिया विश्वविद्यालय में सहायक प्रोफेसर नियुक्त किया गया, जहां वह 2013 तक रहीं। उसके बाद, वह बायोएनटेक आरएनए फार्मास्यूटिकल्स में उपाध्यक्ष और बाद में वरिष्ठ उपाध्यक्ष बनीं। 2021 से, वह सेज्ड विश्वविद्यालय में प्रोफेसर और पेंसिल्वेनिया विश्वविद्यालय के पेरेलमैन स्कूल ऑफ मेडिसिन में सहायक प्रोफेसर रही हैं।
ड्रू वीसमैन (Drew Weissman)

ड्रू वीसमैन का जन्म 1959 में लेक्सिंगटन, मैसाचुसेट्स, अमेरिका में हुआ था। उन्होंने 1987 में बोस्टन विश्वविद्यालय से एमडी, पीएचडी की डिग्री प्राप्त की। उन्होंने हार्वर्ड मेडिकल स्कूल के बेथ इज़राइल डीकोनेस मेडिकल सेंटर में अपना चिकित्सीय प्रशिक्षण और नेशनल इंस्टीट्यूट ऑफ हेल्थ में पोस्टडॉक्टरल शोध किया। 1997 में, वीसमैन ने पेंसिल्वेनिया विश्वविद्यालय के पेरेलमैन स्कूल ऑफ मेडिसिन में अपना शोध समूह स्थापित किया। वह वैक्सीन रिसर्च में रॉबर्ट्स फैमिली प्रोफेसर और आरएनए इनोवेशन के लिए पेन इंस्टीट्यूट के निदेशक हैं।
क्या आप जानते हैं?
- 1901 से अब तक चिकित्सा नोबेल (फिजियोलॉजी या मेडिसिन) में 113 नोबेल पुरस्कार प्रदान किए जा चुके हैं।
- अब तक 12 महिलाओं को चिकित्सा नोबेल पुरस्कार से सम्मानित किया जा चुका है।
- अब तक के सबसे कम उम्र के चिकित्सा नोबेल पुरस्कार विजेता फ्रेडरिक जी बैंटिंग की उम्र 32 वर्ष थी, जिन्हें इंसुलिन की खोज के लिए 1923 में चिकित्सा नोबेलपुरस्कार से सम्मानित किया गया था।
- अब तक के सबसे उम्रदराज़ चिकित्सा नोबेल पुरस्कार विजेता पीटन राउज़ की उम्र 87 वर्ष थी, जब उन्हें ट्यूमर-उत्प्रेरण वायरस की खोज के लिए 1966 में चिकित्सा नोबेल पुरस्कार से सम्मानित किया गया था।
- पिता और पुत्र सुने बर्गस्ट्रॉम और स्वांते पाबो में से प्रत्येक को चिकित्सा नोबेल पुरस्कार से सम्मानित किया गया है। स्वंते पाबो को उनके पिता के 40 साल बाद यह पुरस्कार दिया गया।
नोबेल पुरस्कार विजेताओं का चयन कौन करता है?
अल्फ्रेड नोबेल ने अपनी अंतिम वसीयत में नोबेल पुरस्कार देने के लिए निर्णय लेनेवालों संस्थानों को नामित किया था।
- भौतिकी और रसायन विज्ञान में नोबेल पुरस्कार के लिए रॉयल स्वीडिश एकेडमी ऑफ साइंसेज
- फिजियोलॉजी या मेडिसिन में नोबेल पुरस्कार के लिए करोलिंस्का इंस्टीट्यूट
- साहित्य में नोबेल पुरस्कार के लिए स्वीडिश अकादमी
- नोबेल शांति पुरस्कार के लिए नॉर्वेजियन संसद (स्टॉर्टिंग) द्वारा चुनी जाने वाली पांच व्यक्तियों की एक समिति।
1968 में, स्वेरिजेस रिक्सबैंक ने अल्फ्रेड नोबेल की स्मृति में अर्थशास्त्र में स्वेरिजेस रिक्सबैंक पुरस्कार की स्थापना की। रॉयल स्वीडिश एकेडमी ऑफ साइंसेज को 1969 से शुरू होने वाले अर्थशास्त्र में पुरस्कार विजेताओं का चयन करने का काम दिया गया था।


शानदार
पसंद करेंपसंद करें